La plupart des gens sont familiers avec l'utilisation de mots pour les valeurs numériques telles que "douzaine" pour douze et "paire" pour deux. La chimie utilise un concept similaire avec la taupe (mol en abrégé), qui fait référence non pas à un petit mammifère fouisseur, mais au nombre 6.022 x 10 à la 23ème puissance. Le nombre est beaucoup plus précis que cela, mais pour la plupart des calculs, il est suffisamment précis. Dérivée du nombre d'atomes dans 12 grammes de carbone 12, la mole permet d'utiliser le poids moléculaire d'une substance en tant que facteur de conversion entre moles et grammes d'une substance.
Écris la formule de la substance avec le nombre de moles. Les formules chimiques décrivent le nombre d'atomes pour chaque élément d'une substance. Par exemple, la formule H2O de l'eau indique que chaque molécule contient deux atomes d'hydrogène et un atome d'oxygène. Le nombre de moles pour chaque substance est écrit avant la formule avec les valeurs d'une mole non écrite. Deux moles d'eau sont écrites sous la forme 2 H2O et 1,8 moles d'eau sous la forme 1,8 moles H2O.
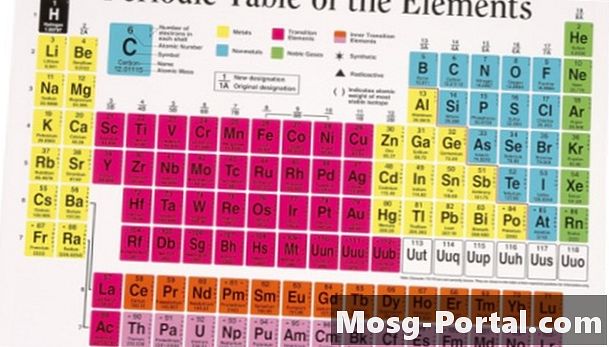
Additionnez les poids atomiques de chaque atome de la molécule pour trouver le poids moléculaire de la substance. Les poids atomiques sont répertoriés dans le tableau périodique sous le symbole de chaque élément. Par exemple, le poids moléculaire de l'eau est obtenu en ajoutant les poids atomiques des deux atomes d'hydrogène et d'un atome d'oxygène dans chaque molécule. Le poids atomique de l'hydrogène est de 1,008 et le poids atomique de l'oxygène est de 16,00; le poids moléculaire est donc de 18,02 (1,008 + 1,008 + 16,00 = 18,02).
Multipliez le poids moléculaire par le nombre de moles pour la substance. Le poids moléculaire est le nombre de grammes par mole pour la substance et donne le facteur de conversion pour les moles en grammes pour cette substance particulière. Ainsi, une mole d’eau a une masse de 18,02 grammes (1 mol d’H2O x 18,02 g / mol = 18,02 g). Deux moles d'eau ont une masse de 36,04 grammes (2 moles de H2O x 18,02 g / mol = 36,02 g). Les fractions de mole sont calculées de la même manière, de sorte que 1,8 mole d’eau ait une masse de 32,44 g (1,8 mole de H2O x 18,02 g / mol = 32,44 g).